北京市重点实验室
消化疾病癌前病变北京市重点实验室
一、重点实验室简介
消化疾病癌前病变北京市重点实验室于2011年6月经北京市科学技术委员会批准成立,依托首都医科大学附属北京友谊医院,以北京市临床医学研究所消化疾病实验研究中心为主体,建立并完善了消化疾病癌前病变相关的基础、临床、转化全链条研究平台,为北京市及全国消化疾病癌前病变领域的医学研究提供技术支撑。
经过近9年的发展,本实验室形成了横跨基础、临床、转化三个层面的研究特色,主要包括:消化道早癌分子机制及肿瘤微环境的基础研究、消化道癌前病变及早癌的内镜介入(微创)临床研究、慢性肝病肝硬化和癌变诊疗的临床研究、消化内镜工程及人工智能辅助诊疗转化研究、消化道肿瘤早诊标记物转化研究。
实验室设有基础平台、临床平台与转化平台,自2012年10月22号新的综合科研平台正式启用以来,实验室已建立核酸提取与纯化、蛋白提取与纯化、Realtime-PCR、蛋白双向电泳、共聚焦显微镜、显微切割、流式细胞术、显微注射、Nano String杂交、毛细管电泳、病理切片扫描系统、二代测序、高内涵细胞检测等一系列科研平台,设备优良,技术先进。实验室在运行期间围绕各个特色研究方向开展了深入研究,在承担国家重大科研项目、成果产出、人才队伍成长和国内外学术影响力等方面取得了一定成绩。

二、人员构成
(1)实验室主任简介
张澍田,博士、主任医师、教授
首都医科大学附属北京友谊医院执行院长
消化系统疾病国家临床医学研究中心主任
国家临床医学研究中心联盟秘书长
科技北京百名领军人才
学术兼职:中华医学会常务理事、中国医师协会常务理事、中国中西医结合学会常务理事、中国医院协会副会长、中国医师协会消化医师分会会长、世界消化内镜学会(WEO)学术指导委员会委员、亚太消化内镜学会委员、国家重点临床专科主任、国家重点学科主任、北京市第12届人大代表、北京市第13届政协常委。
(2)队伍建设和人才培养
目前实验室有科研人员53人,技术人员11人,共计64人,其中正高级职称18人,副高级职称17人,博士生导师6人,硕士生导师15人;实验室科研中坚力量不断壮大,目前包括实验室副主任在内具有学科带头人14名,是实验室创立之初的2倍以上。
学术研究队伍中以中青年骨干(≤45岁)为主,博士学位的人员占75%以上,团队成员涉及消化内科学、分子生物学、细胞生物学、病原生物学、病理学、肿瘤学等多个学科的人才。实验室通过引才、纳才、育才,逐渐形成了一个结构合理、敢于创新、具有良好团队协作精神的学术梯队,为未来实验室快速发展已贮备青年学术人才24人。实验室同时承担了依托单位部分研究生培养工作,自成立以来,实验室共培养博士生27名,硕士生29名。

三、平台简介
(1)基础实验平台
基础实验平台可以支持基本的分子生物学、细胞生物学,病理学实验外,近年来还建立了流式细胞技术平台、显微切割技术平台、激光共聚焦系统平台等高级技术平台。


(2)临床研究平台
目前,临床实验平台建立了消化系统早癌注册登记平台,参与国产消化内窥镜多中心系统评价等大型临床研究,建立了四类消化道相关疾病队列,收集各类标本3万例;目前平台开展研究者发起的临床研究11项、参与公司发起的临床研究10项、承担药物临床观察项目20个,作为组长单位牵头国际药物观察研究2项、牵头国内药物观察研究10项。


(3)科技转化平台
临床转化平台积极参与国产内镜设备及一次性内镜设备研发的相关工作。平台研发的人工智能消化道早癌识别系统优于92%的专业内镜医师,准确率达82%。

三、科研项目及经费支撑
重点实验室目前在研国家重点研发计划3项,国家自然基金8项,北京市科技计划2项,首发基金1项;近5年共承担43个项目,到账总经费2323.2万,主要来源是国家级纵向经费。
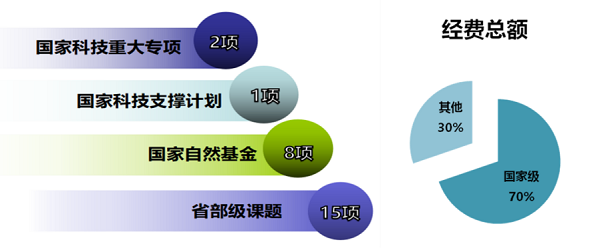
四、研究成果
(1)文章发表情况
2019年度发表SCI论文24篇,年增长20%,累计影响因子83分;IF>5的SCI论文 5篇,IF>10的SCI论文2篇,中科院分区1区3篇,2区4篇。
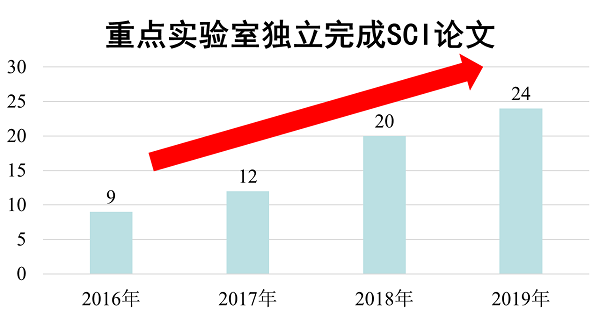
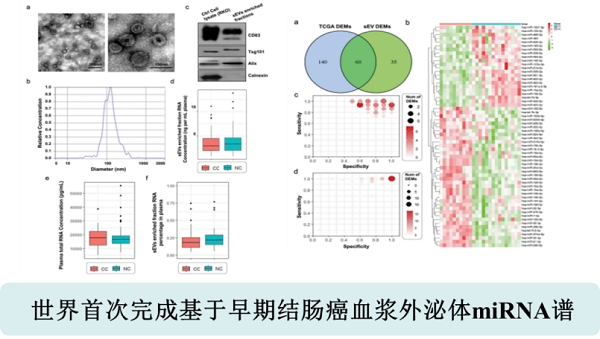
近3年代表性论著
L Min#, S Zhu#, L Chen, X Liu, R Wei, L Zhao, Y Yang, G Kong, P Li*, S Zhang*. J Extracell Vesicles, 2019, 8(1): 1643670. (IF=11.000)
L Min, Y Zhao, S Zhang*. JAMA Surg, 2019, in press. (IF=10.668)
Y Yu, L Chen, G Zhao, H Li, Q Guo, S Zhu, P Li, L Min*, S Zhang*. Oncogene, 2020, 39: 1273–1289. (IF=6.854)
Y Zhao#, Y Yu#, H Li, Z Zhang, S Guo, S Zhu, Q Guo, P Li, L Min*, S Zhang*. Mol Oncol. 2019, 13(5): 1150-1165. (IF=5.962)
M Wang#, L Chen#, Y Chen, R Wei, Q Guo, S Zhu, S Guo, S Zhu, S Zhang*, L Min*. Mol Oncol. 2020, in press. (IF=5.962)
H Li#, Z Zhang#, L Chen, X Sun, Y Zhao, Q Guo, S Zhu, P Li, L Min*, S Zhang*. Cell Death Dis, 2019, 10 (2): 109. (IF=5.959)
Y Yu, S Zhu, P Li, L Min*, S Zhang*. Cell Death Dis, 2018, 9 (10), 961. (IF=5.959)
X Jia, L Min, S Zhu, Z Huang*, S Zhang*. FASEB J, 2018, 32 (10), 5703-5715. (IF=5.498)
(2)专利申报与授权
近三年申报专利15项,其中4项独立获得授权,3项与合作单位共同获得授权,其余8项处于审查阶段。
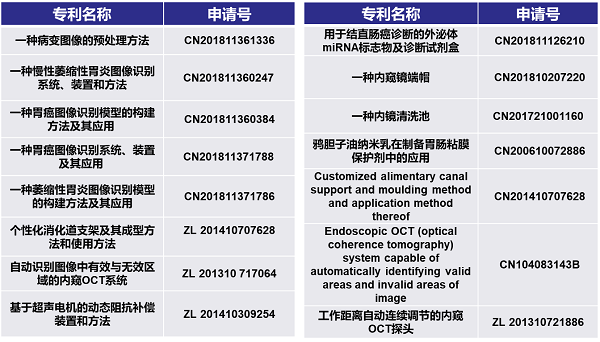
(3)学术地位及影响力
近3年主持编写国家级指南:
《中国结直肠早癌与癌前病变筛查诊治共识》
《中国早期食管鳞癌与癌前病变筛查诊治共识》
《中国巴瑞特食管及其腺癌的诊治共识》
近3年牵头成立国家二级学会:
中国医药质量管理协会临床及大数据质量管理分会
中国卫生信息与健康医疗大数据学会消化专业委员会
中国卫生信息与健康医疗大数据学会消化专业信息标准化委员会
中国卫生信息与健康医疗大数据学会消化疾病诊疗产业工作委员会
五、研究方向简介
(1)方向一:消化道早癌分子机制及肿瘤微环境的基础研究
在消化道早癌分子机制及肿瘤微环境的基础研究方面,我们在流行病学现场及样本库维护、肿瘤关键分子机制研究、微环境研究三个分支方向逐渐深入,取得了一系列的研究进展。
在流行病学现场及样本库维护方面,继续跟进食管癌高发区河北省邯郸市武安县现场(2009年建立)和峰峰矿区现场(2010年建立)的胃镜筛查,覆盖人数达1万余人,随访时间分别达到了11年和10年;此外我们也进一步完善了食管癌高发区高危人群队列以及食管癌前病变样本库,目前样本总量达31万余份。
在肿瘤关键分子机制研究方面,我们继续深入研究ASPN、MGP、FAM175B、NONO、CDK14等一系列关键分子相关机制,依托这些研究进展,2019年度发表了20余篇SCI论文,同时获批了3项肿瘤关键分子机制相关的国家自然科学基金项目资助。微环境研究方向是我们近年来拓展的一个前沿方向,2019年度完善了外泌体分离、鉴定体系、组织来源CAF体外培养体系、结肠类器官培养体系以及3D基因组学分析体系,为后续进一步深入研究早期肿瘤微环境奠定了基础。
(2)方向二:消化道癌前病变及早癌的内镜介入(微创)临床研究
内镜介入(微创)治疗是实验室的重点方向,积极推广多种染色技术,国内首先牵头制定了消化道癌前病变、早期癌的普查筛查技术规范,建立并推广内镜病理标本规范化处理、优化病理技术,探索和初步建立了规范化消化道癌前病变及早期癌的内镜治疗体系。2019年度在内镜介入临床研究方向,获批了2项市科委科技计划重点项目与1项医管局协同中心重点专项,经费总额1280余万元。
为了深入开展多中心、随机对照研究,为早期食管癌、胃癌的规范化诊治提供循证医学证据,并研究高效规范、低成本、具有自主知识产权的新技术,本实验室于2017年5月正式启动了临床科研支撑平台,组建了稳定的临床研究支撑团队,同时与专业的临床研究系统开发公司合作完成了多个疾病的CDE架构,经过近3年的运行,临床研究平台目前已经有“国产消化内窥镜的临床评价”等数十项多中心临床研究在顺利推进,具体包括11项研究者发起的临床研究、10项公司发起的临床研究、20个承担药物临床观察项目、2项作为组长单位牵头国际药物观察研究、10项牵头国内药物观察研究,在全国范围内获得了一定的影响力与综合声誉。
2019年登记并随访胃、食管、结直肠早癌651例,随访率达90%。非肿瘤性疾病登记并随访137例,随访率达90%。依托平台收集1346例各类患者的标本共计13884份,其中冻存组织788份、粪便1964份、血浆6494份、血细胞4638份。2019年临床研究平台开展了10万人的开滦队列的预调查研究,包括胃肠镜筛查意愿及饮食习惯等方面的随访调研;此外也进一步完善了食管癌高发区高危人群队列以及食管癌前病变样本库,目前样本总量达31万余份。
(3)方向三:慢性肝病肝硬化和癌变诊疗的临床研究
在慢性肝病肝硬化及其癌变的诊断及其治疗研究方向,实验室与德国海德堡大学合作,开展了肝硬化门脉高压症的病理生理变化及其机制的研究,并建立以HVPG指导的多学科一体化的肝硬化及其并发症综合救治平台,促进肝病消化、急诊、放射介入、普外、ICU等学科共同发展。探讨和评价临床防治新方法和策略。使肝硬化及其并发症的病死率进一步降低,生活质量提高。主导或参与制定国内肝硬化并发症临床诊治规范或指南。针对进展期肝纤维化、肝硬化患者肝癌早期诊断困难的关键问题,建立了肝癌极高危人群队列,开展了血清学、影像学在原发性肝癌早期鉴别诊断中的临床应用研究,探讨原发性肝癌的危险预测因素。初步建立肝癌早期鉴别诊断体系,肝癌早期诊断达到国际先进水平,BCLC A期占68.8%,单个肿瘤占87.5%。为肝癌患者有机会进行根治性治疗提供了重要保障。研究乙肝相关终末期肝脏疾病患者代谢、病毒变异及分子免疫调节变化,及临床干预方法(药物、消化内镜)。初步建立肝硬化患者药物-内镜微创技术-外科治疗的适宜指标和方法选择。
(4)方向四:消化内镜工程及人工智能辅助诊疗转化研究
以国家消化中心及其两个核心单位为支点,形成了我国最大的消化内镜测试平台,年均内镜检查155,953例,内镜治疗11,485余例;而基于这一大规模的内镜病例数据,我们在消化内镜领域工程研发与科学转化上做了大量的探索性工作。在科技部“十三五”国家重点研发计划——数字诊疗装备研发专项中,作为牵头单位承担课题1项,同时以承担单位参与课题4项,通过医企合作,在消化内镜研发、推广有着丰富的经验积累,2019年度各项任务均平稳推进,圆满完成预期目标。
我们利用依托单位内镜中心电子数据库的10万余例内镜图片、病理结果及临床资料等相关回顾性数据,经过数据洗脱、筛选、内镜专家“背靠背”人工标注等处理,建立了针对“慢性萎缩性胃炎”和“食管、胃、结直肠恶性肿瘤”四种目标病变的训练及测试数据库,囊括了数万张病理活检结果确证有“萎缩”改变的“慢性萎缩性胃炎”数据分库、“食管癌”“胃癌”“结直肠癌”内镜数据分库;进一步对深度学习卷积神经网络(CNNs)中的ZF和VGG16两种模型应用ImageNet中的相关素材进行优化,以适应后续图像的识别任务,开发了能够独立实时识别内镜下消化道早癌与萎缩性胃炎的人工智能系统;经过一年多时间的完善与提升,研发的人工智能系统已在最易漏诊的胃癌中进行测试,以超快的速度、90%以上的准确性,引起社会媒体的广泛关注,2019年度申报国家发明专利5项。
(5)方向五:消化道肿瘤早诊标记物转化研究
在消化道肿瘤早诊标记物转化研究方面,已经完成了较为深厚的工作积累,前期通过对消化道肿瘤基因表达谱分析以及转录因子富集分析等工作,已分别建立了相对健全的各类消化道肿瘤特征性基因Panel及转录调节网络,并从中筛选找到了ASPN、FAM175B、MGP、CDK14等一系列潜在标记物,首次揭示了分泌蛋白ASPN与MGP在细胞内部的功能及作用机制,明确了其作为肿瘤标记物的检测意义,揭示了FAM175B非P53依赖的抑癌功能,相关工作发表在分子肿瘤领域国际权威期刊MolOncol、MolTher-Oncolytics上,受到广泛关注;这些工作也均具有一定的转化潜力,相关专利也正在申报过程中。
2019年我们进一步推进了在液体活检领域的产研合作,与恩泽康泰的外泌体合作项目,对照MISEV2018指南建立了规范化外泌体研究体系,探索并不断优化了UC方法提取外泌体的效率,积累了丰富的外泌体RNA研究经验,在世界上首次完成基于早期结肠癌血浆外泌体miRNA谱的绘制,论文发表在外泌体领域权威期刊JEV上,影响因子11分,相关成果已申报发明专利1项;此外依托国家中心已有的成熟研究成果推广网络,已在四类不同的医疗机构中建立了应用基地,确保项目研发的成果能够得到快速推广。
下一篇: 移植耐受与器官保护北京市重点实验室简介


 微博
微博 微信
微信

 京公网安备11010202008305号
京公网安备11010202008305号